이온성 액체로켓 연료용 테트라졸리윰 유도체의 합성 및 점화지연시간 및 점도에 대한 연구
Synthesis of the Tetrazolium Derivatives for Ionic Liquid Rocket Fuel and a Study of Their Ignition Delay Time and Viscosity
Article information
Trans Abstract
In order to use the liquid rocket fuel, 1,5-diamino-4-methyltetrazolium azide, [DMT]+[N3]- and 1,5-diamino-4-methyltetrazolium cyanide, [DMT]+[CN]- were synthesized and prepared the ionic liquid rocket fuel after dissolving the synthesized solid-type energetic chemicals in hydrazine, respectively. The thermal decomposition temperatures(Td) and densities(d) of the prepared ionic liquid rocket fuels were about 200 ℃ and above 1.0 g/cm3 respectively. The ignition delay times(Idt) of the ionic liqud rock fuels with [DMT]+[N3]- and [DMT]+[CN]- were in a range of 26.6 − 82.5 ms and the 44.0 − 98.5 ms, respectively. These results mean that the synthesized tetrazolium salts could be used as an ionic liquid rocket fuels. The viscosities of the ionic liqud rock fuels with [DMT]+[N3]- and [DMT]+[CN]-, which were dissolved in mixture solution of hydrazine/2-hydroxyethylhydrazine were to be 1.34 − 101 cP, and 1.29 − 80.5 cP, respectively. The synthesized ionic liquid rocket fuels in this study could be used as rocket fuel because the [Idt(100 ms or less), Td(150 ℃ or more), d(1.00 g/cm3 or more), and η(40.0˜ 100 cP)] were achieved to satisfy the range of the used liquid rocket fuels.
1. 서 론
미국은 하이드라진과 비대칭 하이드라진 유도체의 혼합용액과 산화제인 사산화질소를 반응시켜, 타이탄 4호를 발사 성공, 아트라스 발사체는 탄화수소 화합물 RP-1(kerosene)과 액체산소를 반응시켜 성공시키고, 발사체 연료를 액화수소를 사용하여 성공시킨 예가 있다. 중국은 비대칭 하이드라진과 액체수소를 사용한 발사체를 성공한 바가 있으며, 일본은 케로젠과 Aerozine-50 (하이드라진+비대칭 하이드라진 혼합용매)에 액체산소를 산화제로 사용하여 발사체를 성공하였다. 러시아는 비대칭 하이드라진을 원료 산화제를 액체산소를 사용하여 발사체를 성공하였다.
한국항공우주연구원에서는 2010. 03 부터 2021. 03 까지 케로신(등유)을 이용한 한국형발사체를 개발 중이나, 케로신과 같은 탄화수소 연료는 다른 연료에 비해 상대적으로 낮은 비추력을 갖고 있으며, 액체수소와 액체산소를 이용하는 극저온 로켓연료는 저장 및 관리가 매우 어렵고, 밀도가 낮아 큰 저장용량이 요구되며, 별도의 점화장치가 필요하다는 단점을 가지고 있다. 한편, 자동 연소성 이온성 액체로켓연료는 점화장치가 필요 없고, 로켓 엔진 설계가 간단하며, 비휘발성이므로 취급이 용이하며, 밀도가 커서 높은 추진력을 갖는 장점을 가지고 있다[1~5].
이온성 액체 화합물은 청정화학 분야에서 개발된 최대의 산물이며, 고에너지형 이온성액체 로켓추진 연료로의 사용은 선진국에서 활발히 연구를 수행 중이며, 특히 용융 충진용 고폭화약, 자동점화성 청정추진제 등의 분야에 적용 가능성이 높은 것으로 예상하고 있다. 고에너지 함유한 이온성 액체는 국방무기산업의 탄두 미사일, 추진기관, 고성능 폭약 등에 응용성이 기대되며, 민수분야인 우주발사체, 항공분야의 추진체에 산업적 응용성이 매우 크다. 또한, 이온성액체는 이산화탄소 포집 및 저장, 윤활제, 생물화학공학에서 용매, 전기화학의 전해질, 태양전지, 리튬전지 등의 전해질, 유전 및 가스전 개발 시 하이레이트 저해질 등 경제적 및 산업적 필요성이 매우 큰 상황이다.
한편, 액체 로켓연료의 사용 제어를 위해서는 액체연료 및 산화제의 분사 속도와 점화지연시간이 매우 중요한 변수들이다[6~11]. 액체연료탱크와 산화제 탱크에서 일정한 압력과 속도로 파이프를 타고 연소실까지 분사되는 일련의 과정들이 정확히 맞물려야만 정밀한 로켓발사가 가능하다[7].
본 연구에서는 1,5-diamino-4-methyltetrazolium azide 및 cyanide를 합성하였고, 1 H-NMR과 FT-IR로 화학구조를 분석한 후, 이 고에너지화합물을 hydrazine의 용매에 녹여서, 이온성 액체로켓 연료를 제조하고, 이 액체연료에 대하여 열분해 온도, 점도, 점화시간을 평가하여 실제 액체로켓 연료사용 가능성에 대하여 조사하였다.
2. 실 험
2.1 시약 및 기구
Sodium azide, sodium cyanide, iodomethane, 2-hydroxyethylhydrazine, hydrogen peroxide, molecular sieves는 SIGMA-ALDRICH에서 구매하여 사용하였다. Acetonitrile, diethylether, hydrazine monohydrate, cyanogen bromide는 삼전시약에서 구매하였다. 고농도 hydrogen peroxide(90 % 이상)는 본 연구실에서 제조하여 사용하였다. Hydrazine monohydrate는 molecular sieves, 4 Å, 3.2 mm pellet을 이용하여 무수물로 제조하였다. 합성된 염은 1 H-NMR(Inova 600, Varian, USA), FT-IR(Frontier, PerkinElmer, USA), DSC(DSC 204 F1, NETZSCH, Germany), 밀도계(Explorer Pro, MCIK, Korea), 초고속카메라(HDC-F340, COMART SYSTEM, Korea)으로 특성평가 하였다.
2.2 1,5-diamino-4-methyltetrazolium azide and cyanide, ([DMT]+[N3]−) 및 ([DMT]+[CN]−)의 합성
2.2.1 1,5-diaminotetrazole (DAT)의 합성
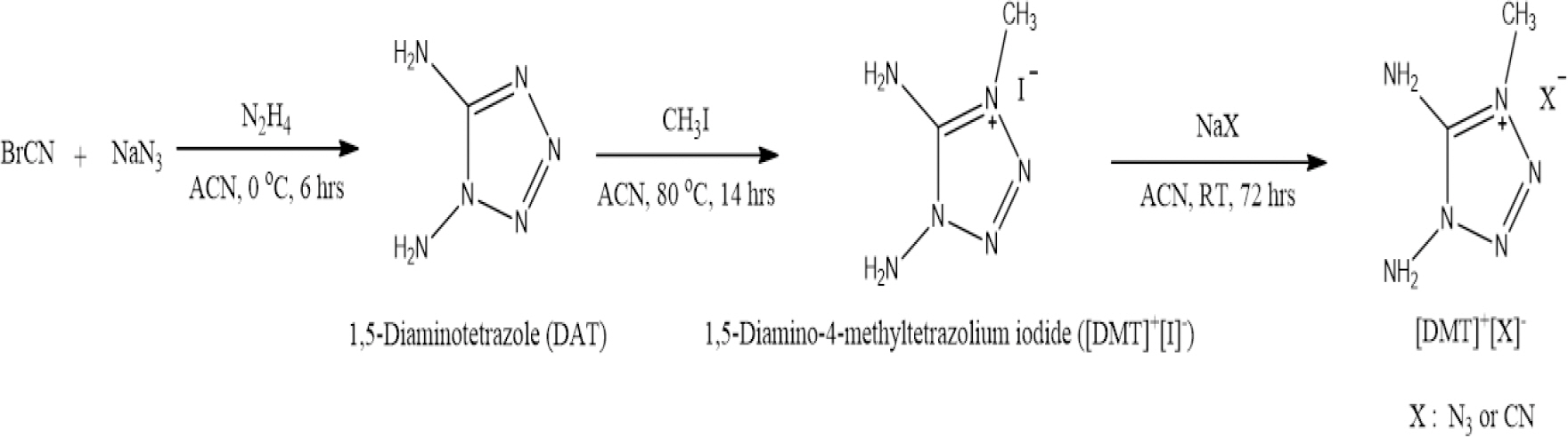
Fig. 1의 DAT의 합성 방법은 문헌[12]을 참조하여 합성하였다. 구체적으로 Two-neck round bottomed flask 에 sodium azide(2.60 g, 40.0 mmol)을 넣고 질소상에 냉각 methanol로 flask 외부를 영하로 냉각시켜주면서, acetonitrile(20 mL)에 cyanogen bromide(1.06 g, 10.0mmol)을 용해시킨 용액을 syringe로 첨가하고 3시간 동안 교반 시켰다. 생성된 NaBr은 감압여과를 통해 제거한 다음, 다시 two-neck round bottomed flask에 여과액을 넣고 냉각시켜주면서 hydrazine monohydrate (0.10 g, 2.0 mmol)을 syringe로 천천히 첨가하고 3시간 동안 교반시킨다. 생성된 흰색 파우더를 걸러낸 다음 diethylether로 충분히 씻어낸 다음 건조시키면 1,5-diaminotetrazole이 얻을수 있었다(수율 85 %).
2.2.2 [DMT]+[I]−의 합성
[DMT]+[I]-의 합성 방법은 문헌[13]을 참조하여 합성하였다. Two-neck round bottomed flask에 1,5-diaminotetrazole(1.5 g, 15 mmol)과 acetonitrile(50 mL)를 넣고 1시간 동안 질소 purge를 시켜준다. 이후 iodomethane(6.4 mL, 90 mmol)을 syringe로 첨가하고 80 ℃에서 14시간 동안 교반시킨다. 생성물은 evaporator 를 이용하여 acetonitrile을 제거한 다음 과량의 diethylether를 넣고 1시간 이상 교반시켜 준 다음 용액을 버리고 diethylether로 충분히 정제하면 [DMT]+[I]-, 가 얻을 수 있었다(수율 92 %).
2.2.3 1,5-diamino-4-methyltetrazolium salts 이온 교환 반응
[DMT]+[I]-와 sodium azide 1:1의 몰수비로 혼합시킨 다음 acetonitrile을 첨가하고 3일 동안 상온에서 교반시켜주면 상대 음이온이 치환된다. 이후 생성물에 과량의 acetonitrile을 가하여 [DMT]+[N3]-를 전부 용해시킨 다음 남은 NaI 염은 여과하여 제거한다. 여과액을 evaporator를 이용하여 감압 증발시켜주면 [DMT]+[N3]- 이 합성할 수 있었다(수율 87 %). [DMT]+[CN]-은 위와 같은 방법으로 합성하였다(수율 83 %)
2.2.4 [DMT]+[I]- 특성평가
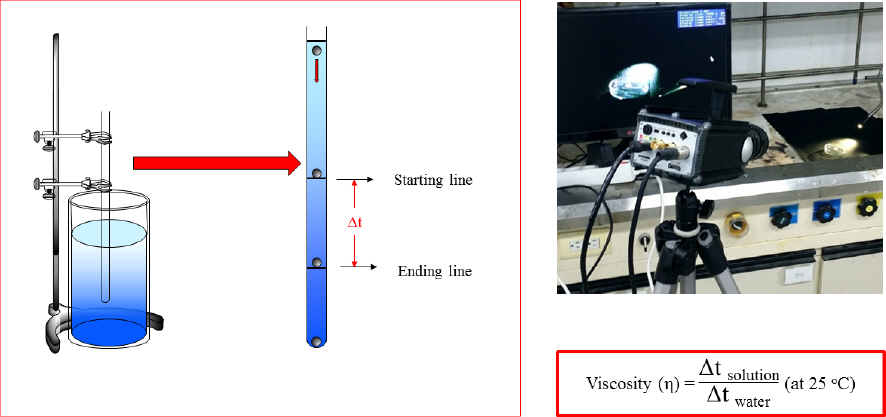
합성된 [DMT]+[I]-의 구조적 특성들은 1 H-NMR과 1 H-NMR은 시료를 FT-IR을 사용하여 확인하였다. DMSO-d₆에 용해시켜 측정하였고, FT-IR은 시료를 KBr 에 혼합시켜 pellet 형태로 만들어 측정하였다. 열적 특성평가는 DSC를 사용하여 질소기체 하에서 5 ℃/min 의 승온속도로 열을 −40 ℃에서 300 ℃까지 측정하였다. Fig. 2에서 농축 과산화수소를 이용한 점화지연시간 측정은 초고속카메라로 초당 1431프레임의 속도로 연속 촬영하여 확인하였고, 점도는 구 낙하점도 측정법을 이용하여 측정하였다.
3. 결과 및 고찰
3.1 분광학적 특성평가
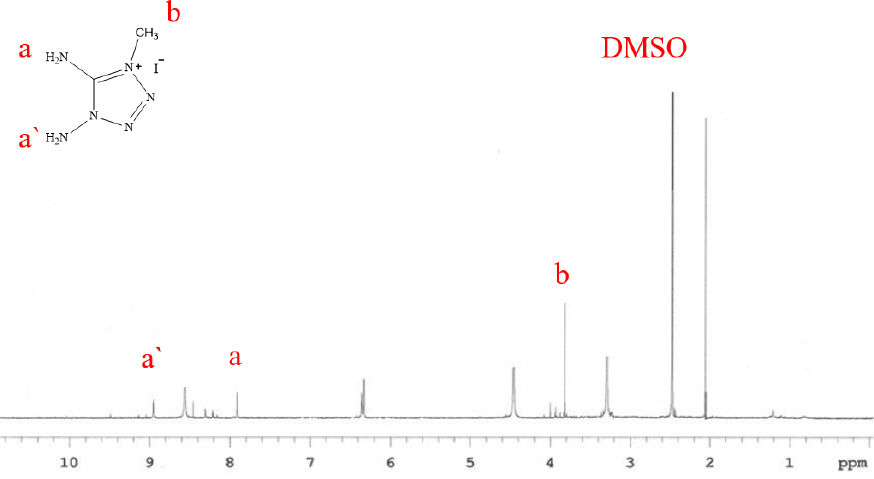
Fig. 3은 1,5-diaminotetrazole의 1 H-NMR 스펙트럼을 나타내고 있다. -NH2의 4개의 수소피이크가 6.4 ppm 부근에서 singlet 나타나서 1,5-diaminotetrazole가 성공적으로 합성됨을 확인할 수 있었다. 1.2와 2.4 ppm에 나타나는 피이크는 DMSO에 들어있는 불순물이라고 생각든다. Fig. 4에서 아민기의 피크가 8, 9 ppm 쉬프트 되었으며, 메틸기의 피크는 3.8 ppm에서 singlet으로 나타난 것으로 보아 고에너지 화합물 전구체인 [DMT]+[I]- 성공적으로 합성되었음을 확인하였다.
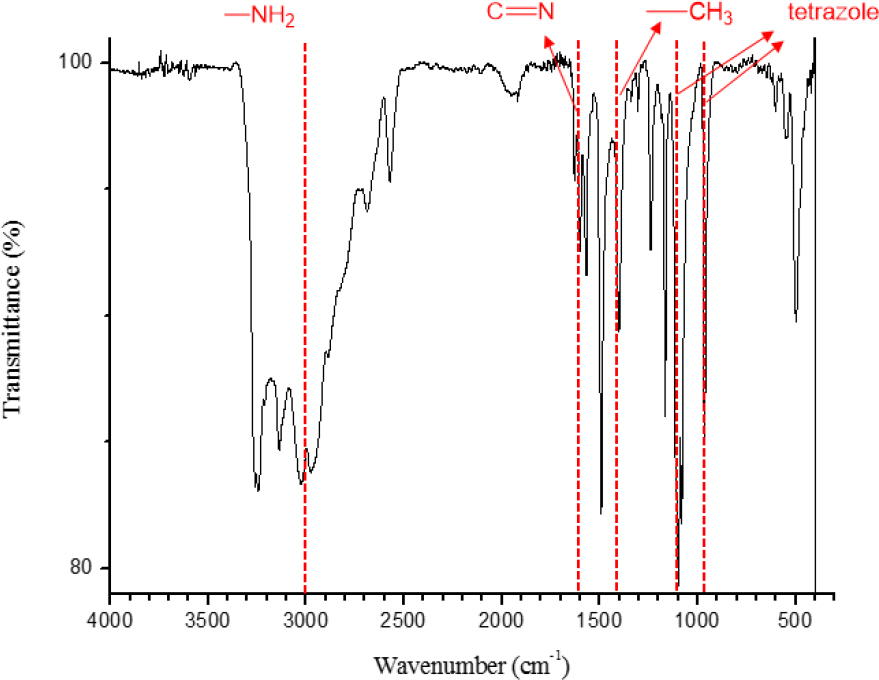
Fig. 5는 합성한 [DMT]+[I]-의 FT-IR spectrum를 나타내고 있다. 여기서, 아민기(-NH₂)의 피크는 3000 cm−1 부근에서, -C = N-의 피크는 1600 cm−1 부근에서, 메틸기(-CH₃)의 피크는 1400 cm−1 부근에서 나타난 것으로 확인되어, 고에너지 화합물 전구체인 [DMT]+[I]-가 제조됨을 확인할 수 있었다.
3.2 열적 특성평가
로켓연료로 사용하기 위하여는 열적 안정성은 매우 중요한 변수 중에 하나이다. 일반적으로 로켓연료로 사용하는 화합물의 열적분해 온도는 150 ℃ 이상이 요구된다. 또한 로켓연료로 사용하기 위하여 화합물은 고에너지를 포함하고 있어야 한다.
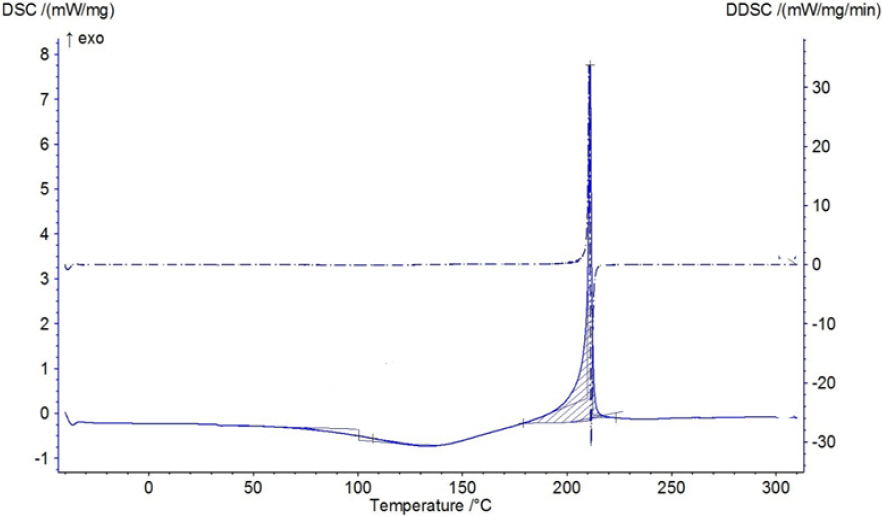
Fig. 6과 Fig. 7은 고체상태 고에너지 화합물 [DMT]+[N3]-와 [DMT]+[CN]-의 DSC 곡선을 나타내고 있다. 고에너지 화합물 [DMT]+[N3]-에서 45 ℃ 흡열 피이크가 나타났는데 고체-고체 1차 상전이로 생각되며, 60 ℃ 부근에서 나오는 작은 흡열 피이크는 2차 상전이 혹은 유리전이 온도로 생각든다. 130 ℃ 나타나는 발열 피이크는 [DMT]+[N3]- 결정구조를 형성하는 피이크로 생각들며 200 ℃에 나타나는 발열 피이크는화학반응(산화반응)에 위한 피이크로 생각든다. Fig. 7의 [DMT]+[CN]-의 고에너지 화합물의 경우 고체-고체 1차 상전이로 생각되는 피이크는 50 ℃ 부근에서 나타났으며, 200 ℃가 넘은 곳에서 커다란 발열 피이크는 화학반응(산화반응)에 위한 것으로 생각든다.
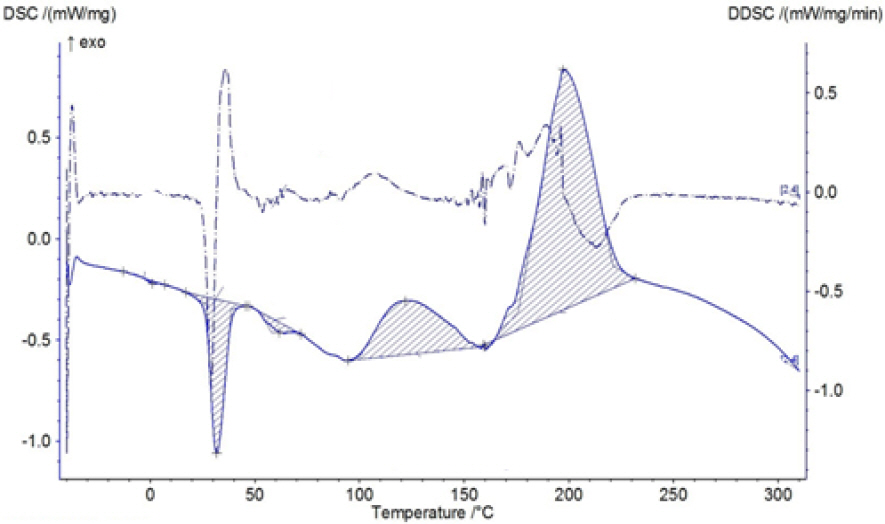
Fig. 8은 [DMT]+[N3]- 고에너지 화합물을 hydrazine 에 농도를 0.2 g/mL 용해 시켜 제조한 이온성 액체로켓 연료의 DSC그래프이다. 결과에서 알 수 있듯이 130 ℃에서 완만한 흡열 피이크가 보여졌는데 이는 고에너지 화합물이 용융되는 것으로 사료되며, 210 ℃이상에서 나타나는 피이크는 화학반응(산화반응), 열분해에 위한 것으로 사료된다. 이러한 결과로서 제조한 이온성 액체로켓 연료로 사용할 수 있다.
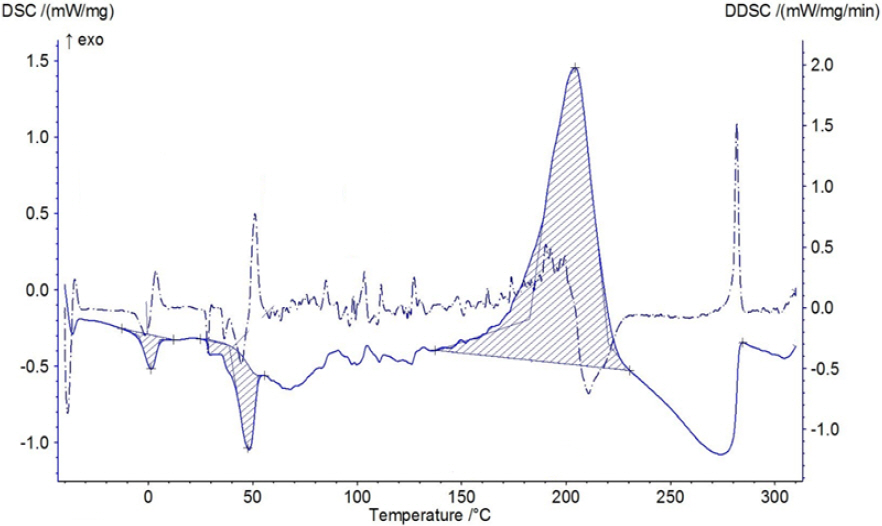
Fig. 9는 합성한 [DMT]+[CN]- 고에너지 화합물을 hydrazine에 농도를 0.2 g/mL 용해 시켜 제조한 이온성 액체로켓 연료의 DSC그래프이다. DSC데이타에서 알 수 있듯이 140 ℃에서 완만한 흡열 피이크가 보여졌는데 이것은 합성한 고체상의 [DMT]+[CN]− 고에너지 화합물이 용융되는 것으로 사료되며, 210 ℃ 이상에서 나타나는 피이크는 화학반응(산화반응), 열분분해에 위한 것으로 사료된다. 이러한 결과로서 제조한 이온성 액체로켓 연료로 사용할 수 있다.
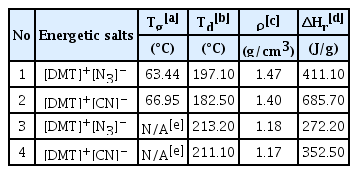
Table 1은 합성한 고체상태의 [DMT]+[N3]- 및 [DMT]+[CN]- 고에너지 화합물과 고에너지 화합물을 2-hydroxyethylhydrazine 용해시켜 제조한 이온성 액체로켓 연료의 물리적 성질을 나타내고 있다. 일반적으로 로켓 연료로 사용하기 위하여는 범위는 Idt(100 mS 이하), Td(150 ℃ 이상), d(1.00 g/cm3 이상), η(40˜100 cP)] 이상위 범위를 달성하여야 한다. 결과에서 알 수 있듯이 이온성 액체추진 연료의 경우 Td 값이 200 ℃, 밀도값이 1.0 g/cm3 이상의 값을 나타내어 충분히 이온성 액체로켓 추진연료로 사용 될 수 있다. 엔탈피의 경우 [DMT]+[CN]-를 함유하는 이온성 액체로켓 연료가 [DMT]+[N3]-를 함유하는 이온성 액체로켓 연료보다 큰 사실을 알 수 있었다.
Table 2는 양자역학적 계산프로그램인 Gaussian 09를 사용하여 합성한 고에너지 화합물인 [DMT]+[N3]-와 [DMT]+[CN]- 물리적 특성들을 계산한 데이터들이다. 결과에서 알 수 있듯이 밀도는 모두 1.0 g/cm3 이상을 가지며, 엔탈피의 크기는 실험값과 동일하게 [DMT]+[CN]-가 [DMT]+[N3]- 보다 크게 나타났다. 이 표에 있는 폭발속도와 폭발압력은 Kamlet-Jacobs equation을 이용하여 계산하였다. 계산값을 바탕으로 한 결과로부터도 합성한 고에너지 화합물 [DMT]+[N3]-와 [DMT]+[CN]-은 로켓 추진연료로 사용 가능성을 나타내고 있다.
3.3 점도 및 점화지연시간 측정
액체로켓 연료로 사용하기 위한 중요한 함 수 중에 하나는 점도 및 점화지연시간이다. Table 3은 초고속카메라를 사용하여 측정한 점화지연시간과 구-낙하 점도측정법을 이용하여 측정한 점도 데이터들이다. 점화지연 시간은 합성한 고에너지 화합물인 [DMT]+[N3]-와 [DMT]+[CN]−을 hydrazine에 용해시켜 이온성 액체로켓 연료를 제조한 다음 90 % 과산화수소를 떨어뜨려 불꽃을 초고속카메라를 통해 확인하였다. 결과에서 알 수 나타나듯이 100 mS 이하였다. 이 결과로서는 제조한 이온성 액체로켓 연료는 로켓 추진제로 충분히 사용할 수 있음을 알 수 있었다. 그러나, [DMT]+[CN]-로 제조한 이온성 액체로켓 연료의 경우 0.1 g/mL 미만의 농도에서는 불꽃이 발생하지 않았다. 농도가 높을수록 점화지연시간은 감소하였다. 각각의 농도에서 점도는 1.5 cP 미만으로 묽은 상태였다. 이 데이터들은 Fig. 9에 도시하였다. 이러한 점도갑은 이온성 액체로켓 연료로의 사용할 수 없음을 의미한다.
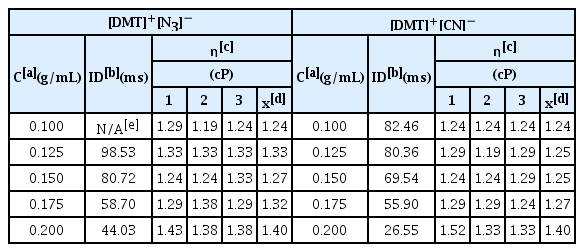
Ignition delay times and viscosities of rocket fuels as function of concentration of the [DMT]+[N3]− and [DMT]+[CN]− in hydrazine
이온성 액체로켓 연료로 사용하기 점도의 범위는 40˜100 cP 범위를 달성해야 한다, 이온성 액체로켓 연료의 점도를 향상시키기 위하여 Table 4와 같이 hydrazine/2-hydroxyethylhydrazine 혼합용매를 제조 후, 고에너지 화합물인 [DMT]+[N3]-와 [DMT]+[CN]-을 용해시켜 점도를 측정하였다. Fig. 10은 혼합용매로 제조한 이온성 액체로켓 연료의 경우 2-hydroxyethylhydrazine의 혼합비율이 높을수록 점도도 높아졌다. 역으로 2-hydroxyethylhydrazine에 hydrazine 을 소량만 혼합시키면 점도는 급격히 감소하였다.

Viscosities of rocket fuels with [DMT]+[N3]− and [DMT]+[CN]− in mixture of hydrazine/ 2-hydroxyethylhydrazine
4. 결 론
이온성 액체로켓 연료를 제조하기 위하여 2종류의 고에너지 화합물, [DMT]+[N3]- 및 1,5-diamino-4-methyltetrazolium cyanide, [DMT]+[CN]-를 합성하고, 합성한 고에너지 화합물을 hydrazine 용매에 용해시켜, 이온성 액체로켓 연료를 제조하였다. 두 종류의 고에너지 화합물을 hydrazine화합물에 용해시켜 이온성 액체로켓 연료를 제조하고, 로켓연료 사용 가능성을 평가한 결과 다음과 같은 결론에 도달하였다.
(1) 액체로켓 연료의 열분해 온도(Td)는 200 ℃ 내외로 안정적으로 로켓연료로 사용할 수 있다.
(2) 액체로켓 연료의 밀도도(d) 1.00 g/cm3 이상으로충분히 로켓연료로 사용 할 수 있다.
(3) 액체연료의 점화지연시간(Idt)은 44.0 − 98.5 ms로서 액체로켓 연료로 사용할 수 있다.
(4) [DMT]+[N3]- 함유한 이온성 액체연료의 점화지연시간은 26.6 − 82.5 ms 이었고, 액체로켓 연료로 사용할 수 있다.
(5) [DMT]+[CN]- 함유한 이온성 액체연료의 점화지연시간(Idt)은 44.0 − 98.5 ms로서 액체로켓 연료로 사용할 수 있다.
(6) hydrazine/2-hydroxyethylhydrazine 혼합용매에 [DMT]+[N3]- 함유한 이온성 액체연료의 점도는 1.34˜101.01 cP 이었고, [DMT]+[CN]- 함유한 이온성 액체연료의 점도는 1.29˜80.5 cP 이었다.
본 연구에서 합성한 이온성 액체로켓 테트라졸염 유도체의 경우, 로켓 연료로 사용할 수 있는 범위 [Idt (100 mS 이하), Td(150 ℃ 이상), d(1.00 g/cm3 이상), η (40.0˜100 cP)]에 달성할 수 있어, 액체로켓 연료로 충분히 사용할 수 있는 결론을 얻었다.